https://tibbigenetikdanisma.blogspot.com
8 Kasım 2020 Pazar
COVID19 Genetik Testleri
15 Temmuz 2020 Çarşamba
Prematür Ovarian Yetmezlik, Erken Menopoz
Prematür Ovarian Yetmezlik (Erken Menopoz)
Genetik nedenlerin ağırlıklı olduğu bir durumdur. Prematür ovarian yetmezliklere (POF, POY) en sık sebep olan genetik neden Turner sendromudur. X kromozomunun bir eksik olması durumudur. Tüm vücut hücrelerinde eksik olabileceği gibi mozaik olarak yani kısmi eksiklikler de söz konusu olabilir. Klasik tip turner sendromunda genellikle folikül rezervi görülmediğinden doğurganlık hiçbir şekilde söz konusu olmaz. Mozaik turner sendromlu hastalarda foliküler kayıp doğum öncesi dönemde gerçekleşmeye başlar bu kişiler adet görüp çocuk sahibi de olabilirler ancak erken yaşta foliküler yetersizlikten dolayı doğurganlık ortadan kalkabilir, erken menopoza girebilirler. Mozaik turner sendromunda prematüre ovarian yetmezlik insidansı yükselmiştir. Menstruel düzenleri normal ancak düşük kan AMH seviyelerine sahip olabilirler. Mozaik turner yüzdesi ve fenotipi çok değişken bir durumdur. Hiçbir bulgu göstermeyebilir. Mozaik turnerdaki en kritik durum mozaik turner olan annenin gonadlarındaki X kromozom eksikliği riski nedeniyle klasik tip turner sendromlu çocuk dünyaya getirme riskidir. X kromozomunu tutan delesyonlar, inversiyonlar, duplikasyonlar, translokasyonlar da prematüre ovarian yetmezlik nedeni olabilir. X kromozomunda lokalize olan DIAPH2 geni, XPNPEP2 geni, DACH2 geni, POF1B geni ve CHM geni ovarian yetmezlikler açısından kritik bölgelerdir.
 |
| Erken Menopoz |
POY’a neden olan 2. Sıradaki genetik neden FMR1 geni mutasyonu ile oluşan Fragile X sendromudur. Bu sendromda FMR1 geni 5’ ucunda CGG trinükleotidlerinin tekrarı sayısal olarak artmıştır. 200’ün üzerindeki tekrarlarda frajil X sendromu görülür Hastalık mental retardasyonla seyreder. 60-199 arası trinükleotid tekrarı olan kişilerde klinik olarak tam fragile X mental retardasyon tablosu görülmez ve bu duruma premutasyon adı verilir. Kadınlarda genellikle taşıyıcılık şeklinde görülen bir durum olup taşıyıcı kadınların erkek çocuklarına %50 oranında hastalık şeklinde aktarılır. Frajil X sendromu mutasyonunu ya da premutasyonunu taşıyan kadınlarda POY görülme sıklığı artmıştır. Özellikle POY başlangıcı ile başvuran ve gebelik isteyen kadınlar bu sendrom açısından araştırılmalılardır ki olası gebelikte hasta bir bebek dünyaya gelmesin. Premutasyon taşıyıcılarında %20 oranında POY ile karşılaşılırken, POY ile başvuran olguların %2-15’inde premutasyon taşıyıcılığı saptanmıştır.
POY’a neden olan bir diğer genetik neden Galaktozemi hastalığı ya da taşıyıcılığıdır. Bu durum galaktoz 1 fosfat üridil transferaz geninin (GALT) mutasyonuna bağlı olarak ortaya çıkar. Otozomal resesif kalıtımlı metabolik bir hastalıktır.
BMP 15 geni, FOXL2 geni ATM geni, STAR geni, EIFB2 geni, POLG geni mutasyonları da prematüre ovarian yetmezliklere neden olabilmektedir.
Tüm bu nedenlerin bir kısmında gebelik ihtimali arttırılabilirken, bir kısmında sadece kadının erken menopoza bağlı kalp ve kemik sağlığını korumaya dayalı tedaviler uygulanabilmektedir.
13 Temmuz 2020 Pazartesi
Genetik
Genetik (kalıtım bilimi) canlılardaki kalıtım ve çeşitliliği inceleyen bir bilim dalıdır. "Genetik" sözcüğünün kökeni ise Yunanca γένεσις - genesis (köken) sözcüğüne dayanır. Kalıtımın aktarım mekanizmalarını çalışan modern genetik 19. yüzyılın ortalarında Gregor Mendel ile başlamıştır.
Genler DNA'nın belli bölgelerine karşılık gelen kalıtım birimleridir. DNA çift zincir bir moleküldür. Bu zincir üzerindeki nükleotitlerin dizisi, canlıların genetik bilgisidir. DNA, iki zincirli bir yapıya sahiptir. Sonraki kuşağa her iki ebeveyne ait birer DNA zinciri kalıtılır. Böylelikle yavrular anne babalarına benzerler ancak anne babalarından farklılıklar da gösterirler. Genetiğin temel görevi benzerlik ve farklılıkların oluşumunun ve aktarılmasının aydınlatılmasıdır. Böylelikle birçok canlı üzerinde açıklanacak olan genetik bilgilerle hastalıkların tanısı, tedavisi, bitki ve hayvanların ıslahı, evrim ve çevreye adaptasyon gibi birçok konu açığa kavuşturulabilinecektir.
DNA,
1. Genetik bilgiyi içerir. (Genetik kod)2. Kendi kendini sentezler. (Replikasyon)
3. Protein sentezi
DNA tüm bu üç görevi sayesinde canlıların yaşamının ve soyunun devamını farklılıkları ve benzerlikleri sağlar.
Genetik kodumuz çevreyle etkileşim halindedir. Çevreye olan tepki yine genotip kontrolündedir. Genotip canlının çevre koşullarına reaksiyon yeteneğini ifade eder. Buna “reaksiyon normu” adı verilir.
Reaksiyon normu üzerindeki araştırmalar, aynı genotipteki farklı çevrelerde büyüyen canlılar ve farklı genotipteki aynı çevre koşullarında büyüyen canlılar arasında araştırılır.
Genotip ve fenotip birbirinden bağımsız olmayan kavramlardır. Evrimin temelini oluşturan bu kavramlar canlılığın adaptasyonunu ve devamını sağlar.
8 Temmuz 2020 Çarşamba
Tıbbi Genetik Uzmanına Nasıl Ulaşırım? Tıbbi Genetik Uzmanından Randevu Alma. Genetik Test Nasıl Yaptırırım?
 |
| Tıbbi Genetik Uzmanı |
Tıbbi Genetik Uzmanı'na yönlendirildiyseniz ya da ulaşmak istiyorsanız ilk etapta mutlaka devletin sağladığı uzmanlarla görüşmeniz sağlık güvencenizi kullanabilmeniz açısından sizin için daha faydalı olacaktır. Çünkü genetik testler maddi anlamda pahalı testlerdir. Hem gereksiz testlerden kaçınmak hem de sosyal güvencenizin sağlayacağı imkanlara ulaşabilmeniz için sağlık bakanlığına bağlı olarak çalışan Tıbbi Genetik Uzmanları'na ulaşmanız sizin için en doğru yol olacaktır. Bunun için https://www.mhrs.gov.tr adresinden giriş yapabilirsiniz ya da telefonla 182'yi arayarak merkezi randevu sisteminden kendinize en yakın Tıbbi Genetik Uzmanından randevu alabilirsiniz. Hekiminize giderken yanınıza şimdiye kadar yapılmış olan tetkiklerinizi almayı unutmayınız. Gebelikle ilgili bir başvuru söz konusu ise randevunuza eşinizle birlikte gitmekte fayda var. Her iki eşten istenecek tetkik ya da muayene söz konusu olabilir. Genetik, tüm aileyi etkileyen bir bilim olduğu için hekiminiz gerek gördüğü durumlarda ailenin diğer fertlerini görmek isteyebilir.
11 Mayıs 2020 Pazartesi
COVİD19, Coronavirüs, Genetik Testi, Real Time PCR
| COVID19 NEGATİF |
 |
| COVID19 POZİTİF |
15 Mart 2020 Pazar
HIV Enfeksiyonunda Genetik, AIDS
HIV (Human Immunodeficiency Virus / İnsan Bağışıklık Yetmezliği Virüsü), AIDS (Acquired Immune Deficiency Syndrome, Sonradan Edinilen Bağışıklık Sistemi Yetersizliği Sendromu) 'e yol açan virüstür.
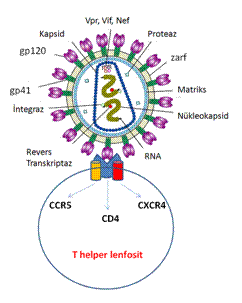 |
HIV |
Milyonlarca insan her yıl HIV’e maruz kalmaktadır, ancak hepsi virüsü almaz, bu da HIV-1 alımında konak genetiğinin potansiyel bir rolü olduğunu gösterir.
HIV alımının polijenik ve kalıtsal olduğunu ispatlayan birçok çalışma mevcuttur. Yapılan çalışmalarda kalıtsallık oranının %28-42 olduğu ve EFHC14 geninin HIV edinimi için yeni bir duyarlılık geni olarak tanımladı. Ayrıca HIV edinimi için duyarlılık varyantlarının T hücrelerinde değil, aynı zamanda striatal ve hipokampal nöronlarda eksprese edilen genler için de önemli ölçüde eksprese olduğu gözlemlenmiştir. HIV edinimi için genetik riskin CXCL17 geni ile ilişkili olduğu tespit edilmiştir.
HIV ile enfekte olunduktan sonra virüsün vücuttaki davranışı yine bireyin genetik yapısıyla ilişkilidir. CNOT1, CNO10, CNOT11 genlerinin farelerde hasara uğratılmasıyla virüsün hücre içine girişinin ve çoğalmasının önüne geçildiği dolayısıyla Th hücrelerin korunduğuna yönelik çalışmalar mevcuttur.
Ayrıca IRF7 geninin HIV alımından korunmaya katkıda bulunduğu ispatlanmıştır. Tüm burada geçen ya da geçmeyen genetik farklılıklar, tedavide, aşı gelişiminde rol alan oldukça önemli değişiklikler ve yolaklardır.
Virüs tek sarmallı RNA’ya sahiptir. RNA ‘yı çevreleyen p24
proteinden oluşan kapsit ve dışında zarftan oluşur. Zarfta antijenik yapyı oluşturan
glikoproteinler bulunur.Virüsün glikoproteinleri aşağıdaki gibidir:• gp160:
Proteaz enzimi ile alt üniteleri olan gp120 ve gp41'e bölünür.• gp41:
HIV'in hücreye girmesini sağlar.• gp120:
HIV'in DNA'ya tutunmasını sağlar.• LEDGF:
HIV'in replikasyonunu sağlar.
14 Mart 2020 Cumartesi
Mitokondri Enjeksiyonu, Tüp Bebek
Mitokondri, hücre içinde yer alan hücrenin oksijenlenmesini sağlayan solunumdan sorumlu bir organeldir. Kendine ait genetik materyali vardır. Mitokondriye ait mitokondriyal DNA anneden kalıtılır.
Hücrenin büyüklüğüne göre sahip olduğu mitokondri miktarı da değişir. Kadın üreme hücresi olan yumurtada mitokondri miktarı diğer büyüklüğü nedeniyle diğer hücrelerimize göre daha fazla sayıdadır. Spermde ise hareket kabiliyeti nedeniyle solunum yani enerji ihtiyacı fazla olduğundan mitokondriler kuyruk bölgesinde toplanmıştır. Spermin baş kısmı yumurtaya girip döllenme başladığında spermin kuyruğu yumurta dışında kalarak kaybedilir. Dolayısıyla çocuğa babadan mitokondri ve mitokondriyal DNA geçişi olmaz.
Mitokondri miktarı yaşla birlikte yumurta hücresinde azalmaktadır. İleri anne yaşı nedeniyle kalitesiz yumurta hücresi nedeniyle gebelik elde edilememesi, başarısız tüp bebek tekrarları gibi durumlarda anne yumurtasındaki mitokondri sayısının arttırılabilirliği üzerine çalışmalar yapılmaya başlanmıştır.
Sadece gebelik değil, bunun dışında yaşlanmayı önleme, çeşitli hastalıkların tedavisinde mitokondri injeksiyonunun kullanılabilirliği üzerine de araştırmalar yapılmaktadır.
 |
Mitokondri ve Mitokondriyal DNA |
Yumurtaya sperm injeksiyonu yapıldığı sırada mitokondriler de yerleştirilir. Yerleştirilen mitokondriler annenin yumurtalığından henüz olgunlaşmamış oositlerinden alınmaktadır. Buna otolog mitokondri injeksiyonu denir.
Bir diğer yöntemse daha genç bir başka anne adayından alınan mitokondri injeksiyonudur. Buna allojenik mitokondri injeksiyonu adı verilir. Ancak bu durumda doğacak bebeğin 3. bir ebeveyni söz konusu olacaktır. Çünkü mitokondriler genetik materyal içeren organellerdir. Bu durum etik açıdan ve mitokondrial DNA ile kalıtılan hastalıklar açısından risk oluşturmaktadır.
Mitokondri injeksiyonu ülkemizde kullanılan bir yöntem değildir. Dünyada ise henüz çok az olguda uygulanmış ve sonuçları hakkında net verilerin henüz elde edilmediği bir yöntemdir. İleri anne yaşı, yumurtaların yaşlanması doğal bir süreçtir bu sürecin önüne geçmek ne kadar doğrudur, ne kadar etiktir ya da bunu ne kadar başarabiliriz gibi sorular mevcuttur. Ayrıca dünyaya yeni gelecek bir bebeğin geleceği üzerinde etki edebilecek yöntemlerin uygulanması ancak bilimsel araştırmaların kesine yakın sonuçlarıyla olmalıdır.
11 Mart 2020 Çarşamba
Likit Biyopsi, Kanser
Kan, ayrıntılı moleküler analize duyarlı iki tip kanser
türevi materyal içerir:
Sağlam tümör hücreleri (CTC'ler) Serbest tümör DNA'sı (cfDNA; dolaşımdaki tümör DNA'sı veya
ctDNA olarak da bilinir)Tümörler hacim olarak arttıkça, fagositlerin apoptotik ve
nekrotik fragmanları ortadan kaldırma ve temizleme kapasitesi artar, bu da
cfDNA'nın kan dolaşımına pasif olarak salınmasına yol açar. Tümörlerin kan
dolaşımına geçmiş olan DNA'sının kandan analiz işlemine likit biyopsi
denilmektedir. Bir diğer adıyla kandan kanser biyopsisidir. Tümör boyutuna ve
vaskülaritesine bağlı olarak, dolaşımda salınan cfDNA miktarı plazmada bulunan
tüm DNA'ların % 0.01 ila% 90'ı arasında değişebilir. Bu nedenle, likit
biyopsiler, tümör dokusu elde etmek zorunda kalmadan tümör moleküler
profillemesine invaziv olmayan bir yaklaşım sağlar. Likid biyopsi aşağıdaki
nedenlerle yapılabilinir.
- Tümör varlığı için tarama;
- Terapi seçimi için (eşlik eden teşhis);
- Tedaviye yanıtı ve ilaç direncini izlemek;
- Cerrahi/rekürrens sonrası minimal rezidüel
hastalığın saptanmasıCTC'lerin ve cfDNA'nın likit biyopsilerde izole edilmesiyle
sağlanan moleküler analizler, kanser hastalarının ilk tanı ve tedavisinde
farklı olaylarda farklı tedavi stratejilerini yönlendirmek için uygulanabilir.
 |
| Likit Biyopsi |
Avantajlar
- Mevcut yöntemlerle belirlenemeyecek kadar küçük tümörlerin tespit edilebilmesini sağlar.
- Tümör belirteçlerinin tanımlanması için invaziv olmayan yöntemdir, biyopsi yapılamayan hastalar için bir alternatif olarak veya ilaç cevabını değerlendirmek için seçenektir.
- Muhtemelen tümör biyopsisi ve analizinden daha az maliyetlidir.
- CTC'lerin ve cfDNA'nın metastazlara neden olan mutasyonların tespitinde, intratümör heterojenliği gibi sorunları atlayarak, tümörün genomik manzarasının doğru bir görüntüsünü sağlar.
- İlaç direnci ve tümör ilerlemesini değerlendirmek için tedavi sırasında seri örnekler elde edebilinir.
- Tümör DNA'sında formaldehitle sabitlenmiş parafine gömülü (FFPE) bloklarda korunduğu doku biyopsisinin aksine, likit biyopsi ile DNA çapraz bağlanması meydana gelmez; böylece tümör DNA dizilemesini kolaylaştırır.
Spermatogenezis, Oogenezis
SPERMATOGENEZİS
Testislerde gerçekleşir. Erkek eşey ana hücresine “spermatogonium” adı verilir. Spermatogonium büyüyerek “primer spermatosit”i oluşturur. Primer spermatosit birinci mayoz bölünme ile “sekonder spermatositler”e dönüşür. Sekonder spermatositler ikinci mayoz bölünmeyi geçirerek “spermatitler”e evrilir. Spermatitler, spermiyogenez sürecinden geçerek hareket edebilen spermler haline gelir. Bu siklusa spermatogenetik siklus denir. 64 gün sürer.
 |
| Spermatogenezis |
OOGENEZİS
Yumurtalar dişi üreme organı olan yumurtalıklarda üretilir. Mayoz ile oluşan yavru hücreler genetik materyalden eşit pay alır ancak sitoplazmayı eşit olarak paylaşmazlar. Oosit ilk mayoz bölünme ile birinci polar cisimciği ve ikincil oositi oluşturur. İkincil oosit, ikinci mayoz sonunda bir adet ootit ve ikinci kutup cisimciği meydana gelir. Ootit daha sonra olgun yumurta hücresine farklılaşır. Spermatogenezden farklı olarak oogenezdeki iki mayoz bölünme sürekli olmaz. Birinci bölünme embriyonun yumurtalıklarında başlar. Ancak profaz I’de durur. Yıllar sonra, yumurta oluşumu başlamadan hemen önce mayoz tekrar başlar. İkinci bölünme ise döllenmeden hemen sonra tamamlanır. Yani bir kadının mayoz 2’si ancak gebelik elde ettiğinde tamamlanmış olur.
 |
| Oogenezis |
Mayoz Bölünme
Genetik materyal miktarı yavru hücrelerde yarıya inmiş olur. Mayoz bölünmeyle haploit sayıda kromozom içeren gametler oluşur. Mayozda homolog kromozomlar çiftli yapılar (sinaps) oluşturur. Sinaps oluşturan her bir yapı bivalent adı alır. Bivalentler dört kromatitten oluşur. (tetrad, dörtlü) Her iki homolog kromozomun da kendini eşlemiş halidir. Haploit duruma gelmek için iki bölünme gerçekleşir.
 |
| Mayoz Bölünme |
MAYOZ 1-İndirgeyici Bölünme: Homolog kromozomlar birbirinden ayrılır. Tetrat olarak bilinen yapı yarıya inerek diyat (iki kromatidli) halini alır.
Profaz 1: Kromatin iplikler kısalıp kalınlaşarak kromozom haline gelir. Homolog kromozom çiftleri sinaps yaparlar. Sinaps yapan kromozomlar arasında krossing-over denen parça değişimi gerçekleşir. Krossing-over genetik çeşitlilik için çok önemlidir.
Profazın Safhaları şu şekildedir.
Leptonema (Leptoten)
Zigonema (Zigoten)
Pakinema (Pakiten): Tetrat görünür hale gelir.
Diplonema (Diploten): Krossing over gerçekleşir.
Diyakinez
Metafaz 1: Her bir tetratın ucunda kiyazmalar görünebilir durumdadır. Kardeş olmayan kromatidleri bir arada tutar. Homolog kromozomlar rastgele kutuplara konumlanır. (kromozomların bağımsız açılımı)
Anafaz 1: Her bir tetradın yarısı ( kardeş kromatidlerin bir çifti) hücrenin kutuplarına doğru çekilir. Homolog kromozomlar ayrılmış olur. Mayoz sırasında ayrılma hataları olabilir. Ayrılmama (non-disjunction) sonucunda n-1 veya n+1 şeklinde kromozom anomalileri oluşur. Bu hatalı gamet döllendiğinde kromozomal anomaliler görülür. (örn: Down Sendromu)
Telofaz 1: Diyatların çevresinde çekirdek zarı oluşur. Kısa bir interfaz dönemine girilir.
MAYOZ 2 -Eşitleyici Bölünme: Kardeş kromatidler birbirinden ayrılır. Diyat olarak bilinen yapı yarıya inerek monad (tek kromatidli) halini alır. Her biri monad içeren, haploit kromozom takımına sahip dört hücre oluşur.
Profaz 2: Diyatların her biri, bir çift kardeş kromatitten oluşmuştur.
Metafaz 2: Sentromerler ekvatoryal düzlemde dizilir.
Anafaz 2: Diyattaki kardeş kromatidler zıt kutuplara çekilir.
Telofaz 2: Her kutupta kardeş kromatid çiftinin bir üyesi kalır.
Sitokinez: Dört adet haploit gamet oluşur.
Mayozun Önemi:
- Diploid hücreler haploit hal alır.
- Krossing over sayesinde gametlerde çeşitlilik sağlanır.
- En önemli çeşitlilik nedeni kromozom ve kromatidlerin ekvatoryal düzleme rastgele dizilimidir.
Hücre Siklusu, Mitoz Bölünme
Canlıların tüm biyolojik faaliyetlerini yürütebilmeleri için genetik materyallerinin olması gerekmektedir. Genetik materyal insanda her bir hücre içinde DNA olarak anne ve babadan alınmış bir çift iplik şeklindedir. Üreme faaliyetinin yaşamın devamı için gerekli olduğu düşünüldüğünde, DNA’mız üreyen yeni hücrelerimize taşınmak zorundadır. Kromozomlar, genetik bilginin aktarılmasında araç olarak kullanılan DNA paketleridir. Bir hücremizin içinde 46 tanedir. Kromozomların gelecek nesillere aktarımı hücre bölünmeleriyle gerçekleşir. Mitoz, kromozom sayısı ana hücre ile aynı olan iki hücre oluşturur. Mayoz, kromozom sayısını yarıya indirir. Kromozomlar sadece mitoz ve mayoz sırasında görülebilir hale gelirler. Bölünme dışında kromozomlar çekirdek içinde bir ağ oluştururlar. Kromozomların bu uzun-ince ağ haline kromatin adı verilir. Çekirdekçik, ribozom, sentriol gibi hücre elemanları, genetik işlev ile yakından ilişkilidir. Mitokondri ve kloroplastlar kendi genetik materyallerine sahiptirler.
Mitoz Bölünme: Vücut hücrelerimizin tamiri sırasında karşımıza çıkan bölünme şeklidir. Yeni hücreler ana hücreler ile aynıdır. Zigotun, mitotik aktivitesi gelişme ve büyümeyi sağlar.
 |
| M:Mitoz, S:Sentez, G1: 1. Büyüme, G2: 2. Büyüme, I:İnterfaz, G0: Dinlenme Fazı |
Karyokinez: Çekirdek bölünmesidir. Genetik materyal iki kardeş hücreye bölünür. Kromozomlar tam olarak kendini eşler, sonra doğru biçimde ayrılır. Sonuçta ana hücreninki ile aynı iki kardeş çekirdek oluşur.
Sitokinez: Karyokinezi izleyen sitoplazma bölünmesidir. Sitoplazma hacmi ikiye ayrılır. Ayrı birer plazma zarı ile çevrilir. Organeller mevcut zar yapılarından yararlanarak ya kendilerini eşlerler ya da yeniden sentezlenirler.
İnterfaz: Hücre bölünmesinin başlangıç evresidir. Mitoz bölünme için kritik biyokimyasal olaylar gerçekleşir. DNA’nın replikasyonu bu safhada görülür.
İnterfazın Evreleri:
 |
| Mitoz Bölünme Safhaları |
Mitozun Evreleri:
Mitoz, dinamik ve süreklilik arz eden bir olaydır. Profaz, Prometafaz, Metafaz, Anafaz, Telofaz safhalarından oluşur.
Profaz:
En uzun safhadır. İki çift sentriol zıt kutuplara doğru hareket eder. Böylelikle sitoplazmik mikrotübüller bir araya gelir ve kutuplar arasında iğ ipliklerini oluşturur. Sentriollerin göçünden sonra çekirdek zarı kaybolur. Kromatin iplikler yoğunlaşmaya başlar. Her bir kromozom bir çift yapı olarak görünür. Bu aşamada kromozomun her bir eşine kardeş kromatid (aynı genetiğe sahiptirler) denir.
Prometafaz ve Metafaz:
Kromozomlar ekvatoryal düzleme hareket eder. Metafaz ise kromozomların ekvatoryal duruşudur. İğ iplikleri kromozomları hareket ettiren, sentromerler ile bir araya gelen kinetokorlara bağlıdır. Kinetokorlar kardeş kromatidleri hücrenin zıt kutuplarına çekmekten sorumludur.
Anafaz:
Mitozun en kısa evresidir. Kardeş kromatidler birbirinden zıt kutuplara doğru göç ederler. Her bir kromatid artık yavru kromozom olarak adlandırılır.
Telofaz:
Mitozun son evresidir. Her bir kutupta iki kromozom takımı vardır. Bu evredeki en önemli olay sitokinezdir. Profazdaki olayların tersi meydana gelir. Kromozomlar çözülmeye başlar. Çekirdek zarı oluşmaya başlar. Telofazın tamamlanmasından sonra hücre tekrar interfaza geçer. İki adet yavru hücre oluşmuş olur.
Hücresel döngü üç nokta tarafından kontrol edilir:
1. G1/S kontrol noktası
2. G2/M kontrol noktası
3. M kontrol noktası
p53 geni G1/M kontrol noktasında görevi olan bir proteindir. Programlanmış hücre ölümü olan apoptoz’dan sorumludur. Kanser vakalarının büyük çoğunluğunda p53 geninde mutasyon mevcuttur. p53’e tümör baskılayıcı gen (tümor supressor gene) adı verilir.
9 Mart 2020 Pazartesi
Göz Renginin Kalıtımı
Göz rengi multifaktöriyel kalıtım gösteren komplike bir özelliktir. Klasik kalıtım yollarını takip etmez. Göz rengi fenotipleri hem epistaz (düzenleyici genlerin varlığı) hem de eksik baskınlık (her iki özelliğin ortalamasının görülmesi) gösterir. Göz renginden sorumlu yaklaşık 16 farklı gen olmasına rağmen, çoğunlukla kromozom 15, bitişik olarak yer alan HERC2 ve OCA2 (oküler albinizm) genleri sorumludur. HERC2'deki bir intron, OCA2’deki promotor etkileşim halindedir. Temelde bu iki genin göz renginde rol aldığı düşünülse de tüm genetik ekspresyonlarda, sapma da meydana gelebilir. Bazı bireylerde, her bir gözde bir tane olmak üzere iki farklı göz rengine sahip olabilir veya tamamen pigmentasyon eksikliği, oküler albinizm görülebilir. Ayrıca, farklı ifadelerin evrimsel etkileri de önemlidir.
Göz renginin daha karmaşık bir kalıtım modeli vardır. Çünkü göz rengi aralıkları, kahverengi, ela, yeşil, mavi, gri ve nadir durumlarda mor ve kırmızı tonlarını içerir. Kahverengi kodlayan bir alelin yeşil veya mavi üzerinde baskın olduğu ve yeşilin mavi üzerinde önceliğe sahip olduğu bilinmektedir.
Stroma ve gözün ön katmanlarındaki melanositler sitoplazmalarında melanini tutar. Vücudun geri kalanında, melanin hücrelerden salgılanır bu yüzden cilt pigmentasyonu yaşam boyunca sürekli değişir. Göz rengi ne olursa olsun, melanosit sayısı farklı değildir. Sitoplazmadaki melanin miktarı ve kalitesi gözün gözlenen rengini belirler. Işık büyük miktarda melaninden geçtiğinde, görünür ışığın çoğu emilir ve geri yansıyan az ışık kahverengi görünür. Göz rengi açıklaştıkça, daha fazla ışık yansıtan hücrelerde daha az melanin bulunur. Kırmızı ve mor gözler pigment eksikliğinden gelir. Kırmızı görünüm, gözün kan damarlarının yansımasıdır. Güçlü bir mavi renk üretmek için çok az pigment olduğunda, kırmızı yansımalar az miktarda mavi ile etkileşerek mor bir renk üretir. Melanozomlar olarak bilinen melanosit spesifik organellerde, melanogenez için iki melanin tipi açığa çıkarır. Biri koyu bir pigment (kahverengi-siyah) olan eumelanin, diğeri ise açık bir pigment (kırmızı-sarı) olan feomelanin’dir.
Membranla ilişkili taşıyıcı protein okülokutanöz albinizm II (OCA2) melanin olgunlaşması için melanozomları taşır. Melanokortin 1 reseptörü (MC1R), bir melanosite üretimi eumelanin ve feomelanin arasında değiştirme talimatı verir. Bu iki protein, hücredeki melaninin kalitesini ve miktarını etkiler. Diğer çok küçük genlerin minik etkileri vardır. HERC2 ve OCA2 göz renginden sorumlu iki ana gendir. OCA2 için destekleyici bölge HERC2 geni içinde bulunur. HERC2'nin intronu 86, OCA2 ekspresyonunu düzenler. HERC2 fonksiyonları ile yapılan çalışmalarda, proteinin pigmentasyonla hiçbir ilgisi olmamasına rağmen delesyonlar hipopigmentasyona neden olmaktadır. Bu bölge ve onun dizisi ile ilgili tek nükleotid polimorfizmindeki (SNP) bir değişikliğin, OCA2 geninin transkripsiyonu için bağlanma alanını düzenleyerek ekspresyonunu değiştirir. SNP, rs12913832, sırasıyla kahverengiden mavi gözlere bir fenotip değişikliğine neden olur. HERC2 içindeki mutasyon durumunda, OCA2 tarafından kodlanan P proteininin ifadesi azalır ve pigmentasyondaki etkilerini etkili bir şekilde azaltır. OCA2 geni ayrıca göz rengi ekspresyonu için çok sayıda bölge içerir. Gen üzerinde göz rengi için 300'den fazla SNP tanımlanmıştır, ancak sonuçlarının sınıflandırılması çok zordur. Gen, kahverengi gözler (BEY2) ve ela gözleri (BEY1) için bir ana kodlama bölgesi içerir. Diğer SNP'ler mavi ve yeşil gözlerle sonuçlanır. HERC2'nin rs1800407 polimorfizmin bu bazın bir C'den T'ye değişimi, kahverengi gözlerden kahverengi olmayan gözlere (genellikle mavi) bir değişikliğe neden olur. OCA2 geni kahverengi gözler için aleller içeriyor olsa bile, HERC2'nin intron 86'sındaki SNP ekspresyonunu önleyecektir. Azalan ifade, eksik hakimiyeti de açıklayabilir. Daha açık kahverengi ve gri tonları, daha açık bir mavi tonu, ikisinin de tamamen baskın olmadığı iki fenotipin bir karışımını gösterir.
Daha önce belirtildiği gibi, melanogenez iki farklı tipte melanin üretir ve çok sayıda protein gerektirir. 11q14-q21 arasında bulunan TYR, melanogenez yolunu başlatır. Bu nedenle, bu proteinlerden herhangi biri doğru şekilde kodlanmazsa, eumelanin üretimi engellenerek daha açık gözler üretebilir. TYR renk kodlamasa da işlev görmeyen bir TYR, pigmentasyondan sorumlu herhangi bir başka geni maskeler.
Sistein esansiyel bir amino asit olmamasına ve eksikliği nadiren ortaya çıkmasına rağmen, eksikliği feomelanin üretimini durdurur. Bir bebekte pigment dağılımı sırasında, sentezlendiği sistein veya metiyoninde düşük bir diyet, amino asit takviye edilene kadar çocuğun gözlerinin rengini etkileyecektir. Bu durumda, pleiotropik etkiler göz rengini değiştirir.
MC1R, yeşil göz elde etme olasılığını artıran bölgeler içerir. Bu gen, kızıl saçlı ve yeşil gözlü insanlarda yaygın ifadesi nedeniyle genellikle 'kızıl başlı gen' olarak adlandırılır. Dopakrom tautomeraz, ela ve yeşil gözler için bölgeler içerir. Açık kahverengi ve ela tonlarında bireylerde eksik hakimiyet görülür. Altın kahverengi bir iris, hem eumelanin hem de feomelaninin karışımını gösterir (sarı rengi üretir) ve ela, gölgeye bağlı olarak genellikle kahverengi ve yeşil veya mavi ve yeşilin bir karışımıdır.
Heterokromi, ciddi bir bozukluk olarak görülmese de birçok kişiyi etkiler. Farklı renkli gözler veya iris içindeki farklı renklerle karakterizedir. Kalıtımsaldır veya hücrelerdeki somatik mutasyonlardan kaynaklanır. MC1R geni tarafından tetiklenen eumelanin / feomelanin anahtarı, bu bozukluğun bazı vakalarını açıklayabilir.
Nüfus çalışmaları temelinde, bilim adamları mavi gözlü mutasyonun Kuzey Avrupa (İskandinav ülkeleri) halklarından kaynaklandığını düşünüyor. Mavi, çoğunlukla Avrupa'dan gelen insanlarla sınırlıdır. Yeşil gözler, muhtemelen genom içindeki kodlama eksikliğinden dolayı, nüfusun en düşük miktarına (bozukluklar hariç) nüfuz eder. Daha birçok gen, kahverengi ve maviyi diğer göz renklerinden daha fazla etkiler. Ayrıca, bir alel kahverengiyi kodlarsa, kritik bir genin kapatıldığı durumlar dışında, bireyin kahverengi gözleri olacaktır. Yeşil gözler maviden daha fazla pigment gerektirir ve kahverengiden çok daha az değildir ve ela tonları (mavi veya yeşil ile kahverengi) daha çok yönlü olduğundan, ela hala yeşilden daha popülerdir.
Tek Gen Hastalıklarında Kalıtım
Otozomal Dominant Hastalıklar:
 |
| Otozomal Dominant Kalıtım |
Otozomal Resesif Hastalıklar:
X’e Bağlı Hastalıklar:
 |
| X'e Bağlı Resesif Kalıtım |





